Tabla Periódica de los Elementos
A medida que se fueron descubriendo los elementos químicos, los científicos intentaron encontrar relaciones entre ellos para poder ordenarlos y así poder estudiar sus propiedades. Sin embargo, fue recién en el siglo XIX, cuando se lograron los primeros resultados. Una de las primeras propuestas la realizó Döbereiner quien analizó las propiedades de los elementos en grupos de tres de ellos, llamadas triadas. Buscaba tres elementos con propiedades químicas similares y luego trataba de encontrar una relación entre las propiedades y los “pesos atómicos” (actualmente masas atómicas relativas) de los elementos.
Más tarde, Newland, propone ordenar los elementos según el valor creciente de pesos atómicos y encuentra que las propiedades de los mismos reaparecen después de intervalos de 8 elementos.
Los pasos definitivos para la clasificación periódica fueron dados por Mendeléev, en 1869. Fue quien propuso por primera vez una Tabla Periódica de los Elementos. En este punto es muy importante que tengas en cuenta que, en esa época, se conocían sólo 63 elementos y que muchos de sus “pesos atómicos” eran incorrectos, por lo tanto, el trabajo de Mendeléev fue realmente muy valioso.
Todas las tablas periódicas que se conocieron posteriormente a la de Mendeléev fueron ligeras modificaciones de ésta, siempre utilizando los “pesos atómicos” como patrón de ordenamiento de los elementos.
Fue recién después que Moseley (1913) formulara el concepto de número atómico cuando se estableció que las propiedades de los elementos dependen fundamentalmente del número de electrones que tenga su átomo y por lo tanto de su número atómico.
La ley periódica actual dice:
La versión actual de la tabla periódica contiene los elementos conocidos, ordenados según el valor creciente de sus números atómicos sin ningún tipo de inversión. Los elementos quedan dispuestos en la tabla, formando hileras horizontales, llamadas períodos y columnas verticales llamadas grupos.
Hay que tener en cuenta que los lantánidos y actínidos deberían ubicarse a partir del lantano y el actinio, respectivamente. No se hace así y se los agrega al final de la tabla, simplemente por cuestiones de comodidad.
PERÍODOS:
- Hasta el momento existen 7 períodos (son las filas de la Tabla Periódica).
- El número del período al cual pertenece un elemento coincide con
la cantidad de niveles de energía en que se ubican los electrones en sus
átomos. Así el H (1s1)
y el He (1s2) están en el período
1, ya que tienen un nivel de energía ocupado con electrones; el Li (1s2 2s1) y el O (1s2 2s2 2p4) tienen dos niveles
de energía ocupados con electrones, por lo tanto, pertenecen al período 2.
GRUPOS:
- En total existen 18 grupos (son las columnas en la Tabla Periódica).
- En cada uno de los grupos se ubican elementos con propiedades
químicas similares.
- Los grupos se encuentran divididos en los subgrupos A y B. A los
elementos que se encuentran en el subgrupo
A se los conoce con el nombre de elementos
representativos, mientras que a los elementos que se encuentran en el subgrupo B se los conoce con el nombre
de elementos de transición. Todos
los elementos que se encuentran en la parte inferior de la Tabla periódica se
los conoce con el nombre de elementos de
transición interna.
- El número romano para el caso del subgrupo A representa el número
de electrones que posee un elemento en el último nivel de energía;
así, por ejemplo, todos los elementos del grupo IA tienen 1 electrón en su
último nivel de energía mientras que los elementos del grupo VIA tienen 6
electrones en su último nivel de energía.
- A los elementos ubicados en el Grupo I se los suele denominar metales
alcalinos, con excepción del hidrógeno (H), que es un NO METAL.
- A los elementos ubicados en el Grupo II, se los denomina metales
alcalinos térreos.
- A los elementos ubicados en el Grupo VIIA, se los denomina halógenos.
- Los elementos de un mismo grupo tienen igual configuración
electrónica externa (CEE), por lo que el
número del grupo al cual pertenece el elemento coincide con el número de
electrones que tienen sus átomos en el último nivel de energía. Para los
elementos representativos, el número de grupo expresado en números romanos (del
IA al VIIIA) coincide con la cantidad de electrones en su último nivel. Por
ejemplo, si realizamos la configuración electrónica del magnesio y el calcio,
obtenemos:
Mg: 1s2 2s2 2p6 3s2
Ca:
1s2 2s2 2p6 3s2 3p6 4s2
Como puede observarse, ambos tienen 2 electrones en el último nivel, por lo tanto, pertenecen al Grupo 2.
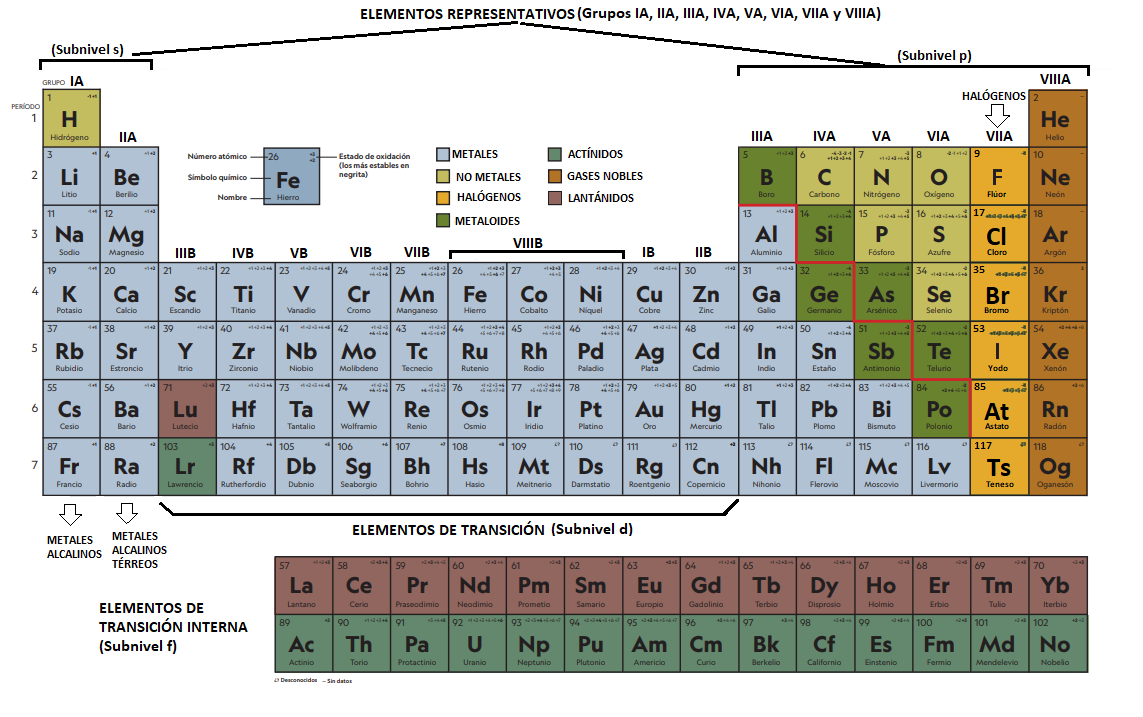
En el link que se encuentra a continuación, podrás encontrar una Tabla Periódica interactiva:
https://ptable.com/?lang=es#Propiedades
PROPIEDADES FÍSICAS DE LOS ELEMENTOS
Los elementos pueden clasificarse en:
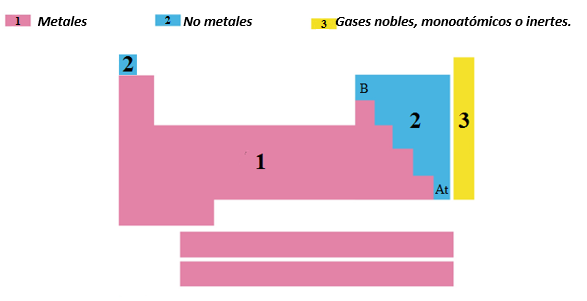
1- Metales: Tienen tendencia a perder electrones y convertirse en cationes. Además, en general:
- Presentan un brillo característico llamado "brillo metálico" que sólo puede
 apreciarse cuando su superficie ha sido recientemente pulida o cortada, dado que tienden a reaccionar rápidamente con el oxígeno del aire formando un óxido metálico opaco.
apreciarse cuando su superficie ha sido recientemente pulida o cortada, dado que tienden a reaccionar rápidamente con el oxígeno del aire formando un óxido metálico opaco. - Son sólidos a temperatura ambiente, a excepción del mercurio que es
 líquido.
líquido. - Son dúctiles y maleables, es decir, se pueden transformar en hilos y láminas delgadas, respectivamente.
- Conducen muy bien el calor y la electricidad.
- Tienen puntos de fusión y ebullición altos.
 apreciarse cuando su superficie ha sido recientemente pulida o cortada, dado que tienden a reaccionar rápidamente con el oxígeno del aire formando un óxido metálico opaco.
apreciarse cuando su superficie ha sido recientemente pulida o cortada, dado que tienden a reaccionar rápidamente con el oxígeno del aire formando un óxido metálico opaco. líquido.
líquido.2- No metales: Al combinarse sus átomos con elementos metálicos, tienen tendencia a ganar electrones y convertirse en aniones. Además, en general:
- Presentan variedad de colores. Por ejemplo, el azufre es amarillo,
el
 bromo es rojo, etc. No presentan brillo metálico.
bromo es rojo, etc. No presentan brillo metálico. - Pueden encontrarse a temperatura ambiente en los tres estados de
agregación (sólido, líquido o gaseoso).
- No son dúctiles ni maleables. Son duros, pero cuando se los golpea
se fragmentan
 con facilidad, es decir, son muy quebradizos.
con facilidad, es decir, son muy quebradizos. - Son malos conductores del calor y la electricidad por ello suelen
utilizarse como aislantes térmicos y eléctricos.
- Tienen puntos de fusión y ebullición relativamente bajos.
 bromo es rojo, etc. No presentan brillo metálico.
bromo es rojo, etc. No presentan brillo metálico. con facilidad, es decir, son muy quebradizos.
con facilidad, es decir, son muy quebradizos.Los no metales se encuentran separados de los metales por una línea imaginaria (“en escalera”) que comienza en el boro y termina en el astato. Corresponde incluir entre ellos al hidrógeno, si bien este elemento tiene, en cierta medida, propiedades peculiares.
3- Gases nobles, monoatómicos o inertes (He, Ne, Ar, Kr, Xe y Rn), también conocidos como gases raros o nobles. Se ubican en el Grupo 18 y se caracterizan por su inactividad química ya que poseen una estructura electrónica estable, por lo que no tienden ni a ganar ni a perder electrones con facilidad. A excepción del helio, todos ellos tienen, en el último nivel, 8 electrones. Los átomos de helio, en cambio, alcanzan una estructura electrónica estable con sólo 2 electrones.

PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS
Las propiedades periódicas son:
- RADIO ATÓMICO
- RADIO IÓNICO
- ENERGÍA DE IONIZACIÓN
- AFINIDAD ELECTRÓNICA
- ELECTRONEGATIVIDAD
A continuación, analizaremos cómo varían las diferentes propiedades de los elementos a lo largo de la tabla periódica.
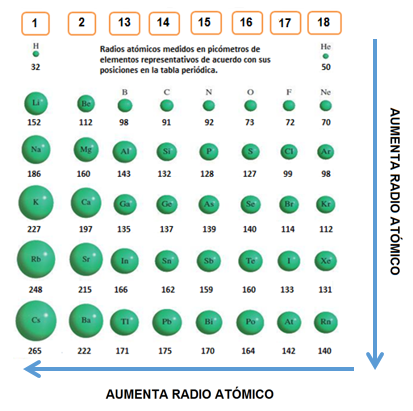
1. RADIO ATÓMICO
Es la mitad de la distancia entre dos núcleos. Es importante tener en cuenta que el concepto de “tamaño de un átomo” no es preciso, ya que la nube de electrones que rodea al núcleo no tiene una frontera definida. Sin embargo, por convención consideraremos los átomos esféricos.
Si nos ubicamos dentro de un mismo grupo, el radio atómico aumenta al aumentar Z, ya que al pasar de un elemento al siguiente a lo largo de un grupo existe una capa más.
Por ejemplo, si consideramos el grupo 1 (Alcalinos), el radio atómico será mayor obviamente para el Francio cuyos electrones más externos se encuentran en el nivel 7 que el Litio cuyos electrones se encuentran en el nivel 2. Al estar en el nivel 7 se encontrará a mayor distancia del núcleo por eso tendrá mayor radio atómico que el Litio.
Si bien la cantidad de protones aumenta de 1 en el Hidrógeno a 87 en el Francio, las capas electrónicas producen un “efecto pantalla” que reduce la atracción que ejerce sobre los electrones el núcleo con cargas positivas.
En un período, el número atómico crece hacia la derecha. Esto significa que un elemento ubicado más a la derecha tendrá mayor cantidad de electrones que su vecino de la izquierda. Al tener más electrones tendrá más protones (cargas positivas). Por lo tanto, habrá más fuerza de atracción de los electrones hacia el núcleo y esto provocará una reducción pequeña del radio atómico ya que la nube electrónica se acercará más al núcleo, en conclusión, los elementos ubicados más a la derecha dentro de un mismo período tendrán menor radio atómico que los ubicados a la izquierda. Por eso, el radio atómico disminuye hacia la derecha.
2. RADIO IÓNICO
El radio iónico es el radio que tiene un
átomo cuando ha perdido o ganado electrones, adquiriendo la estructura
electrónica del gas noble más cercano.
Podemos considerar dos casos:
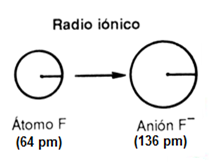
- Que el elemento gane electrones: el electrón o electrones ganados
se colocan en los orbitales vacíos, transformando el átomo neutro en un anión.
La ganancia de electrones por un átomo no metálico aislado es acompañada por un
aumento de tamaño. Al comparar el valor del radio
atómico de cualquier elemento con el de su anión, éste siempre es mayor, dado
que, al aumentar el número de electrones en la capa más externa, también
aumenta la repulsión entre los mismos aumentando de tamaño el orbital
correspondiente y por lo tanto también su radio iónico.
Por ejemplo:
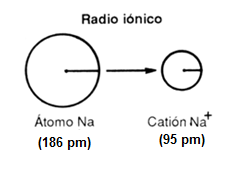
- Que el elemento pierda electrones: se pierden los electrones de la capa más
externa y el elemento se transforma en un catión. La pérdida de electrones por
un átomo metálico implica una disminución de su tamaño. El valor del radio atómico del elemento es
siempre mayor que el del correspondiente catión, ya que éste ha perdido todos
los electrones de su capa más externa y su radio es menor. Por ejemplo:
Por lo tanto, podemos concluir:

Especies isoelectrónicas
Los átomos y
los iones con el mismo número de electrones y distinto número atómico se
denominan isoelectrónicos.
Por ejemplo,
vamos a analizar los iones que forman los átomos de sodio (Na), flúor (F) y
magnesio (Mg). Para ello tendremos en cuenta su configuración electrónica.
Z CE
Na 11 1s2 2s2
2p6 3s1
F 9 1s2
2s2 2p5
Mg 12 1s2
2s2 2p6 3s2
Los iones formados son:
Na+ 1s2 2s2
2p6 (el átomo ha perdido 1 electrón)
F- 1s2 2s2
2p6 (el átomo ha ganado 1 electrón)
Mg2+ 1s2 2s2
2p6 (el átomo ha perdido 2 electrones)
Estos iones Na+, F- y Mg2+
son un ejemplo de especies isoelectrónicas dado que las tres poseen la misma
cantidad de electrones, es decir, la misma configuración electrónica.
¿Qué relación tendrán los
radios iónicos de iones isoelectrónicos?
Estos tres iones
poseen la misma configuración electrónica pero sus radios son diferentes porque
poseen diferente cantidad de protones. El Mg2+ posee la mayor
cantidad de protones; por lo tanto, presenta la mayor atracción de los
electrones y por consiguiente el menor radio. El ión F- tiene la
menor cantidad de protones de los tres iones isoelectrónicos y, como resultado,
presenta el mayor radio.
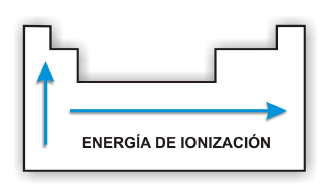
3. ENERGÍA DE IONIZACIÓN
La energía de ionización, es la
energía necesaria para separar al electrón más débilmente unido al núcleo de un
átomo en estado gaseoso, en su estado fundamental. Este proceso puede
representarse por medio de una ecuación como:
Na (g) --> Na+ (g) + e−
La energía de ionización se mide en kJ/mol o
kcal/mol.
En un grupo, la energía de ionización disminuye al aumentar el número atómico, ya que al aumentar el número de capas, los electrones más externos están menos atraídos por el núcleo y, por lo tanto, es menor la energía necesaria para separarlos.
En un periodo, aumenta al aumentar el número atómico, ya que, para la misma capa, a mayor número atómico más atraídos por el núcleo estarán los electrones.
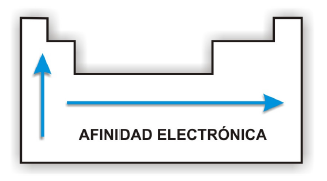
4. AFINIDAD ELECTRÓNICA
Se denomina
afinidad electrónica, a la energía asociada al proceso por el cual un átomo
gaseoso en su estado fundamental acepta un electrón para formar un anión.
Cl
(g) + e− --> Cl− (g)
La afinidad electrónica se mide en kJ/mol o kcal/mol. Los elementos con alta energía de ionización
tendrán gran tendencia a ganar electrones, tendrán afinidades electrónicas
positivas; mientras que los elementos con baja energía de ionización tendrán
poca tendencia a ganar electrones, tendrán afinidades electrónicas negativas.
Por ello, la afinidad electrónica varía en la tabla periódica exactamente igual
que la energía de ionización.
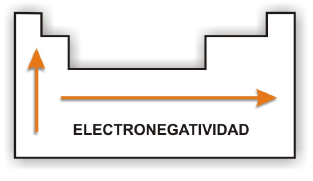
5. ELECTRONEGATIVIDAD
Es la tendencia que tiene un átomo a ganar
electrones cuando participa de una reacción química. Si su electronegatividad
es elevada significa que tiene mucha tendencia a atraer electrones de otro
elemento que sería el dador. Los no metales son aceptores, es decir,
electronegativos y los metales son electropositivos o sea, dadores de
electrones.